Anemias hemolíticas en la infancia
En las anemias hemolíticas, se produce una reducción de la vida media de los hematíes por destrucción eritrocitaria anormalmente elevada (hemólisis).
La médula ósea intenta compensarla aumentando la producción eritroide, respuesta mediada por la eritropoyetina. Como consecuencia, aumenta el porcentaje de reticulocitos en sangre periférica (>2%) y se elevan los índices reticulocitarios.
La bilirrubina no conjugada aumenta por incremento del catabolismo del hemo. Además, se produce disminución de la haptoglobina (alfa-globulina que se fija a las proteínas de la hemoglobina) al ser rápidamente depurada por el sistema mononuclear fagocítico (SMF) sobrepasando la capacidad hepática en la síntesis.
Las manifestaciones clínicas y analíticas dependen de la cuantía y velocidad de la destrucción y del lugar predominante donde ocurre la hemólisis
(Tabla I).
Evolutivamente, pueden aparecer diversas manifestaciones dependiendo de la intensidad del proceso:
Hemoglobina, bilirrubina, diagnóstico.
La hemólisis aguda se produce en el interior de los vasos sanguíneos. Si la cantidad de hemoglobina liberada supera la capacidad de fijación de la haptoglobina, la hemoglobina libre restante atraviesa los glomérulos, es metabolizada por las células tubulares y el hierro resultante se incorpora a las proteínas de depósito (ferritina y hemosiderina).
La presencia de hemosiderina en la orina indica que existe una considerable cantidad de hemoglobina libre circulante que se ha filtrado en el riñón.
Cuando se supera la capacidad de absorción de las células tubulares aparece hemoglobinuria. La existencia de hemoglobinuria es un signo de hemólisis intravascular intensa. Clínicamente, se caracteriza por: palidez, subictericia, taquicardia, debilidad, hipotensión y orina muy oscura.
En los exámenes analíticos, se evidencian anemia aguda, normocítica con reticulocitosis menos intensa que en la hemólisis crónica, ligera hiperbilirrubinemia no conjugada, disminución intensa de la haptoglobina y elevación de la LDH. En la orina, se identifica hemosiderina y hemoglobina.
Clasificación de las anemias hemolíticas(5,6)
De acuerdo con su etiología, las anemias hemolíticas se clasifican en congénitas (intrínsecas) y adquiridas (extrínsecas) (Tabla II).
Anemias hemolíticas congénitas
Anemias hemolíticas congénitas por alteración de la membrana del hematíe(1,2,7,8)
La esferocitosis hereditaria cursa con un síndrome hemolítico crónico sobre el que pueden aparecer crisis aplásicas y crisis hemolíticas.
La membrana del hematíe está formada por una doble capa fosfolipídica y las proteínas integrales y estructurales que constituyen el citoesqueleto (Fig. 1).
Los defectos en la composición proteínica de la membrana producen desacoplamiento entre la bicapa lipídica y el esqueleto, acarreando la pérdida de la forma del hematíe, se reduce su deformabilidad para el paso por áreas de la microcirculación del bazo y una mayor permeabilidad a cationes. Todo esto condiciona una reducción de la vida del eritrocito.
En la tabla III, se resumen los genes que codifican las principales proteínas de membrana y las enfermedades asociadas a sus correspondientes alteraciones.
La esferocitosis hereditaria (EH) es la anemia hemolítica congénita más frecuente en nuestro país. La máxima frecuencia se encuentra en los países del norte de Europa (1 por 5.000 habitantes). La herencia es autosómica dominante en el 75% de los casos y recesiva en el 25%.
Los defectos moleculares más frecuentes son las mutaciones en los genes que codifican la síntesis de la ankirina (mas del 50% de casos) (Tabla III).
La ausencia de interacciones adecuadas del esqueleto del hematíe con pérdida progresiva de elementos de las capas lipídicas por micro vesiculación dan lugar a la forma esferocítica (pérdida de área de superficie sin perder volumen).
Clínicamente la EH puede manifestarse con una gravedad muy variable. Los pacientes afectados pueden permanecer asintomáticos, sin anemia, con hemólisis mínima, detectandose con motivo de estudios familiares o tras presentar una litiasis biliar en la edad adulta (formas leves).
La forma más frecuente de presentación se detecta en los primeros años de vida con anemia, esplenomegalia e ictericia que, ocasionalmente, requiere alguna transfusión (formas moderadas). Muy poco frecuentes son los pacientes con anemia y hemólisis graves, con requerimientos transfusionales frecuentes (formas graves).
Las formas sintomáticas pueden debutar en el periodo neonatal como enfermedad hemolítica no inmune. Puesto que en el recién nacido con EH las pruebas de fragilidad osmótica y el examen morfológico a menudo no son concluyentes, se aconseja realizar seguimiento, estudio familiar y evaluación posterior de los niños con antecedente de hiperbilirrubinemia y anemia neonatal no inmune.
En la evolución de los pacientes con EH, la anemia puede intensificarse y agravarse por varios motivos. Debido al aumento de actividad de la médula ósea, los niños con EH son muy susceptibles a las crisis aplásicas, sobre todo desencadenadas por la infección por parvovirus y a las crisis hemolíticas asociadas a otras infecciones víricas.
En el curso de la enfermedad, la mitad de los pacientes no esplenectomizados sufren litiasis biliar (cálculos de bilirrubinato cálcico).
En la analítica de los pacientes sintomáticos, las tasas de hemoglobina suelen oscilar entre 6 y 10 g/dl. El volumen corpuscular medio es normal, pero la concentración de hemoglobina corpuscular media suele estar aumentada.
Anemias hemolíticas en niños…
En el frotis sanguíneo, se aprecian esferocitos. La fragilidad osmótica está aumentada. Puede completarse el diagnóstico mediante el estudio de las proteínas de membrana de los hematíes y el diagnóstico molecular de las mutaciones genéticas, en laboratorios especializados.
La esplenectomía, por vía laparoscópica, está indicada en las formas moderadas y graves de la enfermedad. Elimina la anemia y la amenaza de las crisis aplásicas, reduce la tasa de reticulocitos y previene los cálculos biliares.
Se aconseja realizarla siempre en niños mayores de tres años y, si es posible, después de los 5 a 9 años. Antes de la cirugía, se administran vacunas frente a gérmenes encapsulados y después profilaxis con penicilina hasta la edad adulta.
Los riesgos y complicaciones de la esplenectomía incluyen las infecciones graves y la tendencia a la enfermedad tromboembólica por la trombocitosis y otros factores. Hasta la esplenectomía, los niños pueden requerir algunas transfusiones y tratamiento con ácido fólico para evitar la reducción de la eritropoyesis.
Anemias hemolíticas congénitas por trastornos enzimáticos del eritrocito(1,2,4,8-10)
Las crisis hemolíticas desencadenadas por agentes oxidantes son características del déficit de glucosa-6-fosfato deshidrogenasa.
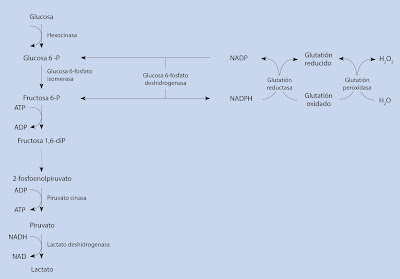
Varios defectos enzimáticos eritrocitarios producen anemias hemolíticas congénitas, siendo los más frecuentes el déficit de glucosa-6-fosfato deshidrogenasa y el déficit de piruvato cinasa (Fig. 2).
En la ruta metabólica del cortocircuito de las pentosas, se produce nicotinamida adenin dinucleótido fosfato reducido (NADPH), reacción mediada por la glucosa-6-fosfato deshidrogenasa (G6PD) (Fig.
2). El NADPH es necesario para mantener el glutatión reducido,que protege la hemoglobina de la acción oxidativa del peróxido de hidrógeno. Cuando disminuye el glutatión reducido, la hemoglobina desnaturalizada precipita (cuerpos de Heinz) y se produce la hemólisis.
anemias hemoliticas
Esta deficiencia enzimática tiene una herencia ligada al cromosoma X, afecta a más de 200 millones de personas en el mundo y es un ejemplo de “polimorfismo equilibrado”, por la ventaja evolutiva de resistencia al paludismo falciparum en las mujeres heterocigotas, que contrarresta el pequeño efecto negativo de los varones hemicigotos afectados. Se ha clonado y secuenciado el gen responsable y están descritas más de 100 variantes enzimáticas distintas.
Clínicamente, el déficit de G6PD es responsable de dos síndromes clínicos: una anemia hemolítica episódica intravascular inducida por agentes oxidantes y una anemia hemolítica crónica espontánea no esferocítica.
Las tres variantes más frecuentes del enzima que dan lugar a crisis hemolíticas desencadenadas por agentes oxidantes son la africana, la mediterránea y la oriental.
Los síntomas aparecen uno o dos días después de haber ingerido las sustancias oxidantes (aspirina, sulfamidas, primaquina, vitamina K, habas frescas, etc.) o de iniciarse una infección vírica o bacteriana.
En las formas graves, la anemia intensa puede poner en peligro la vida. Los cuerpos de Heinz aparecen durante las crisis y, como las células que los contienen son eliminadas con rapidez de la circulación, pueden dejar de verse después de 2 ó 3 días.
Es frecuente que la primera manifestación de un déficit de G6PD sea en forma de ictericia neonatal, más aún si a la madre antes del nacimiento o al recién nacido se les administran fármacos oxidantes.
El diagnóstico depende de la demostración de la disminución de actividad del enzima en los eritrocitos, más evidente después de varias semanas del episodio hemolítico, cuando remite la intensa reticulocitosis, porque las células jóvenes poseen una actividad enzimática mayor.
La mejor medida terapéutica es la prevención de los episodios hemolíticos en los pacientes predispuestos evitando la exposición a agentes oxidantes. La esplenectomía en las formas de hemólisis crónica no está generalmente indicada.
Deficiencia de piruvato cinasa
En la deficiencia de piruvato cinasa (PK) se altera la generación de ATP y los eritrocitos no pueden mantener su contenido de agua y de potasio, se vuelven rígidos y su vida media disminuye. La deficiencia de PK se hereda como un trastorno autosómico recesivo y se debe a mutaciones del gen PKLR localizado en el cromosoma 1q12.
Las personas homocigotas presentan reducción marcada de la actividad PK en los eritrocitos o la producción de un enzima anormal con actividad disminuida.
Generalmente, se asocia a un síndrome hemolítico crónico, con tasas de hemoglobina entre 8 y 12 g/dl, en general sin necesidad de transfusiones. El diagnóstico precisa la demostración de una marcada reducción de la actividad PK eritrocitaria. En estos pacientes está indicada la esplenectomía.
Anemias hemolíticas congénitas por alteraciones de la hemoglobina(2,4,11-14)
En la talasemia, existe déficit de producción de una de las cadenas de globina; en la drepanocitosis, una sustitución de un aminoácido por otro en la globina.
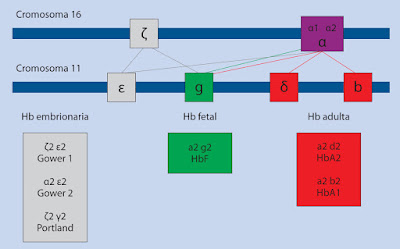
La hemoglobina A1 del adulto es una hemoproteína trimétrica (a2:ß2). El gen estructural de la a-globina está duplicado (a1 y a2) y se encuentra en el cromosoma 16, por lo que cada célula diploide contiene 4 copias.
Existe un solo gen funcional de la hemoglobina en el cromosoma 11, por lo que la célula diploide tiene dos genes (Fig. 3).
En la actualidad, aproximadamente un 5% de la población mundial es portadora de un gen de la hemoglobina potencialmente patológico.
Como los portadores sanos (25% en algunas poblaciones) se encuentran protegidos frente a los efectos mortales del paludismo, estas anemias hereditarias estaban inicialmente confinadas a las regiones tropicales y subtropicales, donde presentan una alta incidencia. El aumento mundial de las migraciones ha introducido las hemoglobinopatías en muchas zonas donde originalmente no eran endémicas.
Talasemias
Son un grupo de enfermedades genéticas, de herencia autosómica recesiva, que se caracterizan por una reducción en la síntesis de uno de los dos tipos de cadenas globínicas, creando un desequilibrio entre ambas, que condiciona la disminución de la vida media del hematíe.
Dependiendo del tipo de cadena de globina afectada, se denominan alfa o betatalasemias. El término talasemia se deriva del griego “talaza”, que significa mar, debido a la alta frecuencia en los individuos que viven alrededor del Mediterráneo.
Alfa Talasemias
Se conocen más de 30 mutaciones o deleciones que afectan a uno o a los dos genes de a-globina. Dado que las cadenas alfa son necesarias para la eritropoyesis fetal y la producción de Hb F, las alfa talasemias pueden ser sintomáticas intraútero.
La presencia de dos genes a condiciona la presencia de las combinaciones genotípicas que se correlacionan con fenotipos clínicos específicos dependiendo de la capacidad de síntesis de cadenas (Tabla IV): deleción de los cuatro genes: (–/–) (Hydrops fetalis). Deleción de tres genes: (–/-a) [enfermedad de la HbH (ß4)].







5 Comments
Pingback:
Pingback:
Pingback:
Pingback:
Pingback: